Was sind eigentlich Wasserstoffbrückenbindungen, wie kommen sie zustande und wo spielen sie eine Rolle?
Über diese Frage könnte man Bücher schreiben (es wurden ja auch einige geschrieben), hier wollen wir sie kurz und überblicksmäßig erklären:
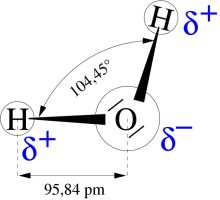
Wasserstoffbrückenbindungen sind am einfachsten im Fall von Wasser (H2O) selbst zu verstehen, in dem zwei Wasserstoffatome an ein Sauerstoffatom gebunden sind; da das Sauerstoffatom einen viel größeren Kern besitzt, ist es elektronegativer, zieht seine Elektronen also stärker an sich; es ist sogar so elektronegativ, dass es Elektronen aus den benachbarten Wasserstoffen abzieht, das als leichtestes Element überhaupt sehr schnell seine Elektronen zumindest partiell verlieren kann. So entsteht eine partielle Negativladung im Sauerstoff und eine partielle Positivladung (durch Elektronendefizienz) in den Wasserstoffatomen - ein elektrischer Dipol ist entstanden.
Wie überall im Leben ziehen sich auch in der Chemie Gegensätze an - und ein partiell positiv geladenes Wasserstoffatom aus einem Wassermolekül fühlt sich nun zu einem partiell negativ geladenen Sauerstoffatom aus
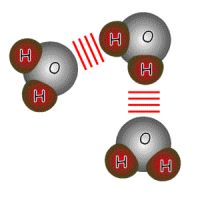 einem benachbarten
Wassermolekül hingezogen, eine "Brücke" zwischen den
beiden
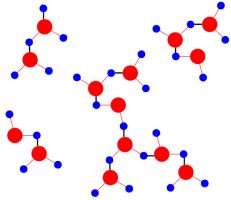
Molekülen hat sich gebildet - ein wahres Netzwerk aus
Wasserstoffbrücken entsteht.
einem benachbarten
Wassermolekül hingezogen, eine "Brücke" zwischen den
beiden
Molekülen hat sich gebildet - ein wahres Netzwerk aus
Wasserstoffbrücken entsteht.Die Bindungsenergie dieser Wasserstoffbrückenbindungen liegt mit 21kJ/mol in einem "magischen Bereich", über jenen Energien der Van der Waals-Kräfte oder hydrophoben Wechselwirkungen, die so schwach sind, dass bereits thermische Fluktuationen ihnen ein Ende bereiten können und deutlich unter den rigiden kovalenten Bindungen in Molekülen, die nur durch enorme Energiemengen gelöst werden können; diese Art der Bindung besitzt also genau jene Flexibilität, die in biologischen Systemen von Nöten ist und rasche Lösung/Bildung von Bindungen ermöglicht. Dadurch, dass sich die Energie mehrerer Bindungen addieren, werden Polymere, die durch zahlreiche Wasserstoffbrückenbindungen verbunden werden (z.B. DNA) äußerst fix 'verleimt', obwohl die Einzelbindung nicht besonders stark ist; trotzdem können sie problemlos wieder aufgeschmolzen werden, wenn sie transkribiert oder translatiert werden müssen.
Aber es wird noch besser...
 Wasserstoffbrückenbindungen
sind aber nicht auf
Wasser alleine beschränkt. Überall, wo zwei partielle
Dipole
aufeinander treffen, können sich diese anziehen und
festhalten, am
häufigsten betrachtet man dies in biologischen Systemen, neben
der
schon bekannten Sauerstoff-Wasserstoff'bindung' die
Stickstoff-Wasserstoff'bindung'; je nachdem, an welchen anderen Atomen
die Stick- und Sauerstoffe "hängen", ist der Dipolcharakter
stärker oder schwächer ausgeprägt,
dementsprechend
stärker oder schwächer ist die
Wasserstoffbrücke, sodass extreme Feinjustierung
möglich ist.
Wasserstoffbrückenbindungen
sind aber nicht auf
Wasser alleine beschränkt. Überall, wo zwei partielle
Dipole
aufeinander treffen, können sich diese anziehen und
festhalten, am
häufigsten betrachtet man dies in biologischen Systemen, neben
der
schon bekannten Sauerstoff-Wasserstoff'bindung' die
Stickstoff-Wasserstoff'bindung'; je nachdem, an welchen anderen Atomen
die Stick- und Sauerstoffe "hängen", ist der Dipolcharakter
stärker oder schwächer ausgeprägt,
dementsprechend
stärker oder schwächer ist die
Wasserstoffbrücke, sodass extreme Feinjustierung
möglich ist.Im Fall der vier Basen der DNA, Adenin, Cytosin, Guanin und Thymidin, sind es spezifische Wasserstoffbrückenbindungen, ihre unterschiedliche Anzahl und ihre sterische Ausrichtung, die dafür sorgen, dass nur Adenin mit Thymidin und Cytosin mit Guanin paaren kann, was im Grunde erst das geniale Prinzip der DNA ermöglicht - nämlich, dass durch einen Strang komplementär der zweite erstellt werden kann - das Prinzip von Replikation und Transkription...
Life, Everywhere!
 Wo also spielen
Wasserstoffbrückenbindungen
ihre besondere Rolle? Einfach überall! Sie sorgen für
die
Besonderheit des Wassers, in dem uns bekannten Bereich flüssig
vorzukommen (gäbe es keine
Wasserstoffbrückenbindungen
wäre Wasser bei Zimmertemperatur gasförmig!), sie
sorgen
durch ihre Bindungskraft nach dem Reißverschlussprinzip
für
das Zusammenhalten der DNA und für die Informationsspeicherung
durch die Anzahl der Bindungen. Besondere Bedeutung erzielen
Wasserstoffbrückenbindungen auch bei der Faltung von Proteinen
und
RNA-Strängen in ihre 3D-Konformation, da
Wasserstoffbrückenbindungen zwischen
Aminosäureseitenketten
bzw. RNA-Basen für die Stabilisierung der Form sorgen, indem
sie
ihr Festigkeit gegen thermische Schwankungen bieten.
Wo also spielen
Wasserstoffbrückenbindungen
ihre besondere Rolle? Einfach überall! Sie sorgen für
die
Besonderheit des Wassers, in dem uns bekannten Bereich flüssig
vorzukommen (gäbe es keine
Wasserstoffbrückenbindungen
wäre Wasser bei Zimmertemperatur gasförmig!), sie
sorgen
durch ihre Bindungskraft nach dem Reißverschlussprinzip
für
das Zusammenhalten der DNA und für die Informationsspeicherung
durch die Anzahl der Bindungen. Besondere Bedeutung erzielen
Wasserstoffbrückenbindungen auch bei der Faltung von Proteinen
und
RNA-Strängen in ihre 3D-Konformation, da
Wasserstoffbrückenbindungen zwischen
Aminosäureseitenketten
bzw. RNA-Basen für die Stabilisierung der Form sorgen, indem
sie
ihr Festigkeit gegen thermische Schwankungen bieten.Auch wenn das nur ein verschwindend geringer Abriss der Bedeutung der Wasserstoffbrückenbindungen war, erkennt der geneigte Leser doch sofort ihre zentrale Bedeutung für sämtliche Prozesses der Biologie, so dass man mit Fug' und Recht behaupten kann, dass ohne diese bedeutungsvollen Bindungen kein Leben, wie wir es kennen, denkbar ist...